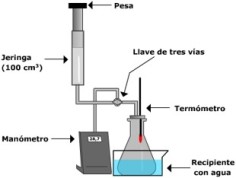
- Nesta ligazón podes explorar que sucede a nivel molecular cando modificamos o volume, a presión e a temperatura dun gas. Se este gas é ideal, responde ás Leis de Boyle-Mariotte (T=cte), Gay-Lussac (V=cte) e Charles (P=cte).

1-Vai á pestana “Leyes” e investiga en “Boyle”, “Charles” e “Gay-Lussac”.
2-A continuación, preme en “Laboratorio” e vai a “Sala Boyle” e “Sala Charles”
- Estoutra ligazón interactiva tamén ilustra as leis dos gases.
1-Observa o movemento das partículas ao incrementar a temperatura na primeira pestana.
2-Na pestana “Ley de Boyle” toma parellas de datos P,V e comproba que se cumple a lei de Boyle.
3-Na pestana “Lei de Gay Lussac” toma parellas de datos P,T e comproba que se cumple a lei de Gay Lussac.